कोशिका चक्र
कोशिका चक्र या कोशिका विभाजन चक्र घटनाओं का एक समूह है जो एक कोशिका का दो संतति कोशिकाओं में विभाजन सुनिश्चित करता है।
कोशिका जीवन की इकाई है। जीवन में निरंतरता बनाए रखने के लिए कोशिकाओं को विभाजित होते रहना पड़ता है। किसी व्यक्ति के विकास और चोटों की मरम्मत के लिए भी कोशिका विभाजन की आवश्यकता होती है।
कोशिका के विभाजित होने से पहले, उसे निम्नलिखित चीजों को सुनिश्चित करना होता है:
-
इसमें बढ़ने के लिए पर्याप्त पोषक तत्व (विकास संकेत) हैं।
-
इसने अपने आनुवांशिक पदार्थ (डीएनए) की प्रतिकृति बना ली है।
-
इसके डीएनए को कोई नुकसान नहीं पहुँचा है।
एक कोशिका एक सफल कोशिका विभाजन सुनिश्चित करने के लिए कोशिका चक्र से गुजरती है।
कोशिका चक्र के चरण
कोशिका चक्र घटनाओं की एक क्रमबद्ध श्रृंखला है जिसके परिणामस्वरूप एक कोशिका दो संतति कोशिकाओं में विभाजित हो जाती है। यह 4 चरणों से बना है।
- G1 चरण (विकास चरण 1)
- S चरण (संश्लेषण चरण)
- G2 चरण (विकास चरण 2)
- M चरण (माइटोसिस या विभाजन चरण)
यदि कोशिका के पास बढ़ने के लिए पर्याप्त संसाधन नहीं हैं, तो वह कोशिका चक्र से बाहर निकलकर G0 (मैं इसे G नॉट के रूप में उच्चारित करता हूँ) नामक विश्राम चरण में जा सकती है।
कोशिका चक्र के पहले तीन चरण - G1, S और G2 को एक साथ इंटरफ़ेज़ कहा जाता है। इसलिए, कोशिकाएँ अपना अधिकांश समय इंटरफ़ेज़ में बिताती हैं, M चरण में विभाजित होने से पहले अपने डीएनए को दोहराती हैं।
आइये प्रत्येक कोशिका चक्र चरण के बारे में थोड़ा और समझें।
G1 चरण
कोशिका चक्र के G1 चरण में, एक कोशिका अपने डीएनए की प्रतिकृति बनाने के लिए तैयार होती है। आस-पास के माध्यम में वृद्धि कारक जिन्हें मिटोजेन्स कहा जाता है, कोशिका की सतह पर रिसेप्टर्स द्वारा पहचाने जा सकते हैं। यह कोशिका को अधिक mRNA और प्रोटीन का उत्पादन करके बढ़ने की अनुमति देता है। mRNA का उत्पादन डीएनए के प्रतिलेखन द्वारा किया जाता है। इस mRNA का उपयोग अनुवाद नामक प्रक्रिया द्वारा प्रोटीन बनाने के लिए किया जाता है।
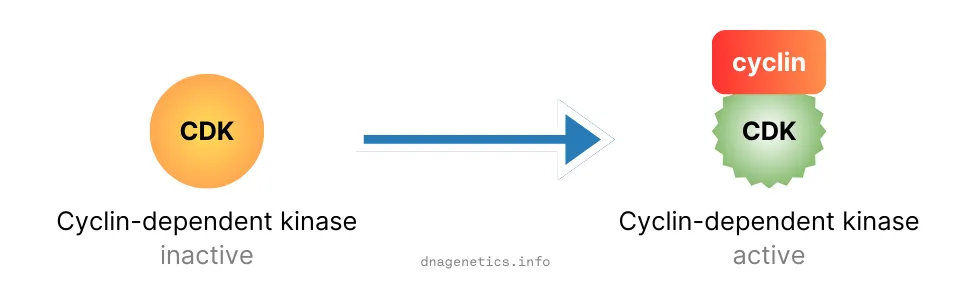
इन प्रोटीनों को कोशिका चक्र नियामक भी कहा जाता है। इस श्रेणी के प्रमुख प्रोटीन साइक्लिन और साइक्लिन आश्रित किनेसेस (CDKs) हैं। साइक्लिन और CDK को कोशिका चक्र का मुख्य चालक माना जाता है। वे कोशिका चक्र के सकारात्मक नियामक हैं। इसके विपरीत, कोशिका चक्र के नकारात्मक नियामक भी मौजूद हैं। उदाहरण के लिए, कोशिका चक्र जाँच बिंदु कोशिका चक्र को नकारात्मक रूप से विनियमित करते हैं।
विशिष्ट CDK को उनके साथी साइक्लिन द्वारा सक्रिय किया जाता है। सक्रिय CDK ऐसे एंजाइम होते हैं जो फॉस्फोरिल समूह (PO3) को अन्य प्रोटीन में जोड़ने को उत्प्रेरित कर सकते हैं। इसे फॉस्फोरिलेशन कहा जाता है।
G1 में, साइक्लिन D मुख्य साइक्लिन है। यह CDK4/6 को सक्रिय करता है जो रेटिनोब्लास्टोमा प्रोटीन (Rb) को फॉस्फोराइलेट करता है।
Rb का फॉस्फोरिलेशन कोशिका चक्र के आगे बढ़ने के लिए एक सकारात्मक संकेत है। यह साइक्लिन E के उत्पादन का संकेत देता है, जो CDK2 को सक्रिय करता है। यह कोशिका के लिए अगले चरण, S चरण या संश्लेषण चरण में आगे बढ़ने का संकेत है।
CDK2 गतिविधि कोशिका चक्र के एक नकारात्मक नियामक, APC/C (एनाफ़ेज़ प्रमोटिंग कॉम्प्लेक्स/साइक्लोसोम) को हटा देती है। APC/C माइटोसिस के एनाफ़ेज़ चरण को बढ़ावा देता है, लेकिन G1 में इसे हटाने की आवश्यकता होती है, ताकि कोशिका S चरण में आगे बढ़ सके। APC/C को हटाना कोशिका चक्र में एक प्रतिबंध बिंदु है। एक बार APC/C हटा दिए जाने के बाद, कोशिकाएँ अपरिवर्तनीय रूप से S चरण में प्रवेश करने, अपने डीएनए की प्रतिकृति बनाने और दो संतति कोशिकाओं में विभाजित होने के लिए प्रतिबद्ध हो जाती हैं।
G1 में, कोशिकाएँ प्रतिकृति के मूल की पहचान करके और उसे चिह्नित करके डीएनए प्रतिकृति के लिए भी तैयार होती हैं। मनुष्यों जैसे जीवों में, जिनका जीनोम बहुत बड़ा होता है, कोशिकाओं को अपने डीएनए की प्रतिकृति बनाने के लिए प्रतिकृति के कई मूल की आवश्यकता होती है।
S चरण
कोशिका चक्र के एस चरण में, डीएनए जीनोम की एक प्रति बनाने के लिए प्रतिकृति बनाई जाती है। डीएनए प्रतिकृति कोशिका के डीएनए को डीएनए की एक नई, समान प्रतिलिपि बनाने के लिए टेम्पलेट के रूप में उपयोग करती है।
G1 के अंत में सक्रिय CDK2 कोशिकाओं को डीएनए प्रतिकृति की शुरुआत को बढ़ावा देकर एस चरण में धकेलता है।
एस चरण के अंत के बाद, द्विगुणित गुणसूत्र (संख्या में 46) दोगुने होकर 92 हो जाते हैं।
मानव जीनोम अनुक्रम ३२०० करोड़ बेस पेयर लंबा है। एस चरण में, इस पूरे डीएनए अनुक्रम की प्रतिलिपि बनाई जाती है ताकि एक समान, डुप्लिकेट डीएनए अनुक्रम बनाया जा सके।
हमारे जैसे जटिल जीनोम में, प्रतिकृति के कई मूल से डीएनए की प्रतिकृति बनाई जाती है। प्रत्येक मूल पर, डबल-स्ट्रैंडेड डीएनए को दो सिंगल-स्ट्रैंडेड डीएनए अणुओं में खोला जाता है। इनमें से प्रत्येक एकल-रज्जुक डीएनए का उपयोग पूरक डीएनए स्ट्रैंड को संश्लेषित करने के लिए टेम्पलेट के रूप में किया जाता है। नव संश्लेषित संतति डीएनए स्ट्रैंड पैतृक डीएनए टेम्प्लेट की एक समान प्रतिलिपि होगी।
G2 चरण
डीएनए प्रतिकृति पूर्ण होने के बाद, कोशिकाएं G2 चरण में बढ़ना जारी रखती हैं। कोशिकाएं डुप्लिकेट किए गए डीएनए को अलग करने के लिए तैयार होती हैं। यह प्रक्रिया CDK द्वारा भी मध्यस्थता की जाती है।
G2 में, CDK2 गतिविधि चरम पर होती है और साइक्लिन B (G2 साइक्लिन) के उत्पादन को प्रेरित करती है। साइक्लिन B CDK1 को सक्रिय करता है, जो माइटोसिस के लिए आवश्यक प्रोटीन को सक्रिय करके कोशिकाओं को माइटोसिस के लिए तैयार करता है।
समसूत्री विभाजन
माइटोसिस में, एस चरण में दोहराए गए गुणसूत्र अंततः दो संतति कोशिकाओं में विभाजित हो सकते हैं।
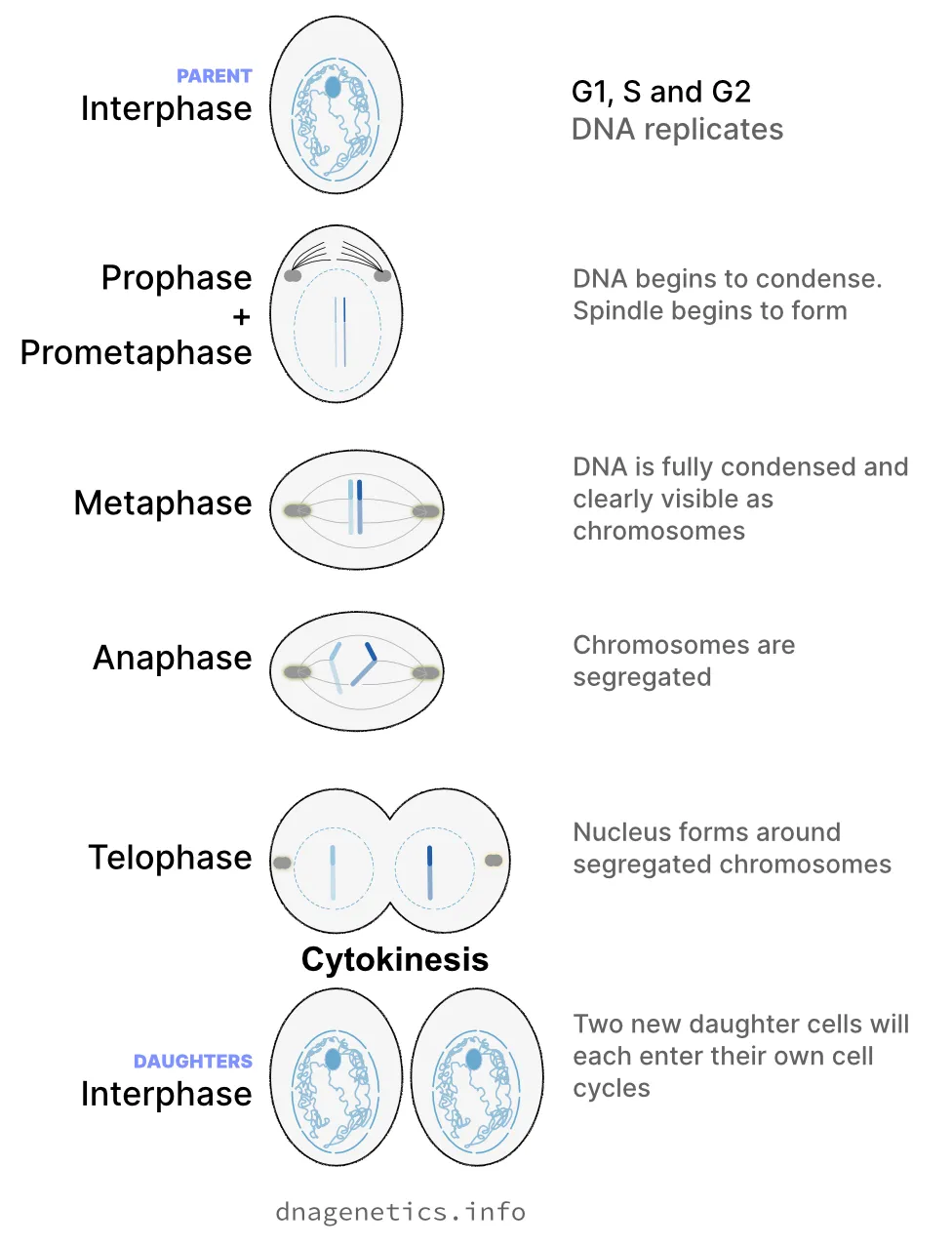
माइटोसिस को उप-चरणों में विभाजित किया जाता है:
- प्रोफ़ेज़ - डीएनए गुणसूत्रों में संघनित होना शुरू हो जाता है
- प्रोमेटाफ़ेज़ - धागे जैसे तंतु जिन्हें स्पिंडल कहा जाता है, बनते हैं और गुणसूत्रों से जुड़ते हैं
- मेटाफ़ेज़ - डीएनए पूरी तरह से संघनित होता है और गुणसूत्रों के रूप में दिखाई देता है
- एनाफ़ेज़ - गुणसूत्रों को स्पिंडल तंतुओं का उपयोग करके कोशिका के दो विपरीत पक्षों में विभाजित किया जाता है
- टेलोफ़ेज़ - कोशिका के प्रत्येक पक्ष पर गुणसूत्रों के चारों ओर एक नाभिक बनता है
साइटोकाइनेसिस
माइटोसिस के बाद, कोशिका में दो नाभिक बनते हैं। ऐसी कोशिका को द्विकेंद्रकीय कोशिका कहा जाता है।
टेलोफ़ेज़ के बाद और साइटोकाइनेसिस के दौरान, एक द्विकेंद्रकीय कोशिका दो संतति कोशिकाओं में विभाजित हो जाती है। इससे कोशिका चक्र पूरा हो जाता है। नवगठित संतति कोशिकाएँ एक नए कोशिका चक्र में प्रवेश कर सकती हैं।
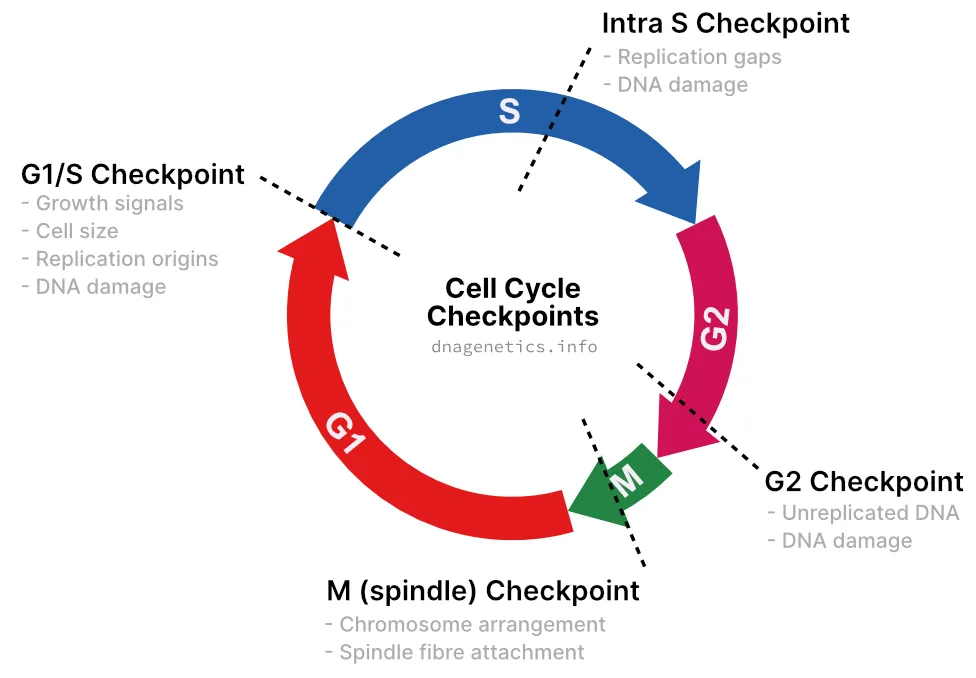
कोशिका चक्र जांच बिंदु
कोशिका चक्र जांच बिंदु (सेल साइकिल चेकपॉइंट) एक सेलुलर सिग्नलिंग मार्ग है जो संकट की स्थिति में कोशिका चक्र को रोक देता है। यह साइक्लिन और CDK सहित चेकपॉइंट प्रोटीन द्वारा मध्यस्थ होता है। एक अन्य लोकप्रिय कोशिका चक्र जांच बिंदु प्रोटीन p53 है।
कोशिका चक्र के विभिन्न चरणों में जांच बिंदु मौजूद होते हैं।
G1/S संक्रमण के दौरान एक जांच बिंदु मौजूद होता है। यह जांच बिंदु कोशिका चक्र के G1 से S चरण में संक्रमण के दौरान DNA क्षति की निगरानी करता है। यदि यह जांच बिंदु सक्रिय होता है, तो कोशिकाएँ G1 में रुक जाएँगी और S चरण में प्रवेश नहीं करेंगी। G1 जांच बिंदु भी CDK और p53 द्वारा मध्यस्थ होता है। कोशिका चक्र के लंबे समय तक रुकने से एपोप्टोसिस नामक कोशिका आत्मघाती प्रक्रिया सक्रिय हो जाएगा।
हालाँकि, एक बार G1 जांच बिंदु पार हो जाने के बाद, कोशिका अपरिवर्तनीय रूप से विभाजन के लिए प्रतिबद्ध हो जाती है। इसका मतलब है कि G1 जांच बिंदु को पार करने वाली कोशिका G0 चरण में प्रवेश नहीं कर सकती।
S चरण में DNA प्रतिकृति की निगरानी करने वाले जांच बिंदु को इंट्रा-S-चरण जांच बिंदु कहा जाता है। यह सुनिश्चित करता है कि DNA संश्लेषण के दौरान कोई ‘अंतराल’ न रह जाए।
G2 में, यदि कोई अप्रतिकृति या क्षतिग्रस्त डीएनए पाया जाता है, तो जांच बिंदु सक्रिय हो जाता है। यह G2 जांच बिंदु है। यह कोशिका चक्र को रोकता है और क्षतिग्रस्त डीएनए में मरम्मत प्रोटीन को भर्ती करता है। एक बार डीएनए क्षति की मरम्मत हो जाने के बाद, जांच बिंदु बंद हो जाती है और कोशिका चक्र फिर से शुरू हो सकता है।
माइटोसिस में जांच बिंदु को M जांच बिंदु या स्पिंडल जांच बिंदु कहा जाता है। यह उचित गुणसूत्र व्यवस्था की जाँच करता है। यह यह भी सुनिश्चित करता है कि उचित पृथक्करण के लिए स्पिंडल फाइबर गुणसूत्रों से जुड़े हुए हैं।
यहाँ कोशिका चक्र चेकपॉइंट का सारांश दिया गया है।
G1/S जांच बिंदु
- विकास संकेतों और कोशिका आकार की निगरानी करता है
- प्रतिकृति और डीएनए क्षति की उत्पत्ति की निगरानी करता है
इंट्रा एस जांच बिंदु
- प्रतिकृति के दौरान डीएनए क्षति की निगरानी करता है
G2 जांच बिंदु
- अप्रतिकृतिकृत और क्षतिग्रस्त डीएनए की निगरानी करता है
M जांच बिंदु (धुरी जांच बिंदु)
- गुणसूत्रों की उचित व्यवस्था पर नज़र रखता है
- स्पिंडल फाइबर के सही जुड़ाव पर नज़र रखता है

कोशिका चक्र अवधि
कोशिका चक्र के प्रत्येक चरण की अवधि विभिन्न प्रकार की कोशिकाओं में भिन्न होती है।
एक सामान्य मानव कोशिका चक्र लगभग 24 घंटे तक रहता है। G1 9 से 11 घंटे तक रहता है। S चरण 8 से 10 घंटे तक रहता है। G2 लगभग 4 घंटे और माइटोसिस लगभग एक घंटे तक रहता है।
इंटरफ़ेज़ कोशिका चक्र का सबसे लंबा चरण है।
सारांश
इस लेख में, मैंने कोशिका चक्र का एक परिचयात्मक अवलोकन प्रस्तुत किया है। मैंने संक्षेप में कोशिका चक्र के चरणों का वर्णन किया और प्रत्येक चरण में क्या होता है। इसके अलावा, मैंने यह भी बताया कि साइक्लिन, सीडीके और कोशिका चक्र के अन्य नियामकों द्वारा कोशिका चक्र को कैसे विनियमित किया जाता है। फिर मैंने कोशिका चक्र जांच बिंदुओं का परिचय दिया और बताया कि वे कोशिका के विभाजन से पहले गुणवत्ता नियंत्रण जांच के रूप में कैसे कार्य करते हैं। ये जांच अगली पीढ़ी में उत्परिवर्तन को पारित होने से रोकने में मदद करती हैं।
यह लेख उन पाठकों के लिए है जो अभी कोशिका चक्र के बारे में सीखना शुरू कर रहे हैं। मुझे उम्मीद है कि मैंने कोशिका चक्र का एक व्यापक अवलोकन प्रदान किया है।
